Российский биолог намерен отредактировать геном эмбриона, чтобы избавить ребенка от наследственного заболевания. Что может пойти не так?
Биолог Денис Ребриков планирует отредактировать геном ребенка, чтобы тот избежал наследуемой глухоты. Для этого ученый хочет изменить определенный ген в эмбрионе, полученном методом ЭКО от двух слабослышащих родителей – они согласились быть добровольцами в этом эксперименте.
До сих пор в мире была сделана только одна попытка генетического редактирования эмбриона человека. Китайский ученый Цзянькуй Хэ внес изменения в гены двух девочек от анонимной пары, чтобы снизить у них риск возникновения ВИЧ. Однако редактирование оказалось неудачным, и российский биолог планирует пойти по принципиально иному пути. Заведующий лабораторией редактирования генома Научного центра гинекологии, акушерства и перинатологии имени Кулакова Денис Ребриков уверен, что его команда впервые в мировой истории сможет избавить ребенка от заболевания с помощью редактирования генома.
«Такие дела» поговорили с ученым, чтобы узнать, почему он считает возможным то, что не удалось пока никому в мире, и его коллегой, который считает такой эксперимент преждевременным.
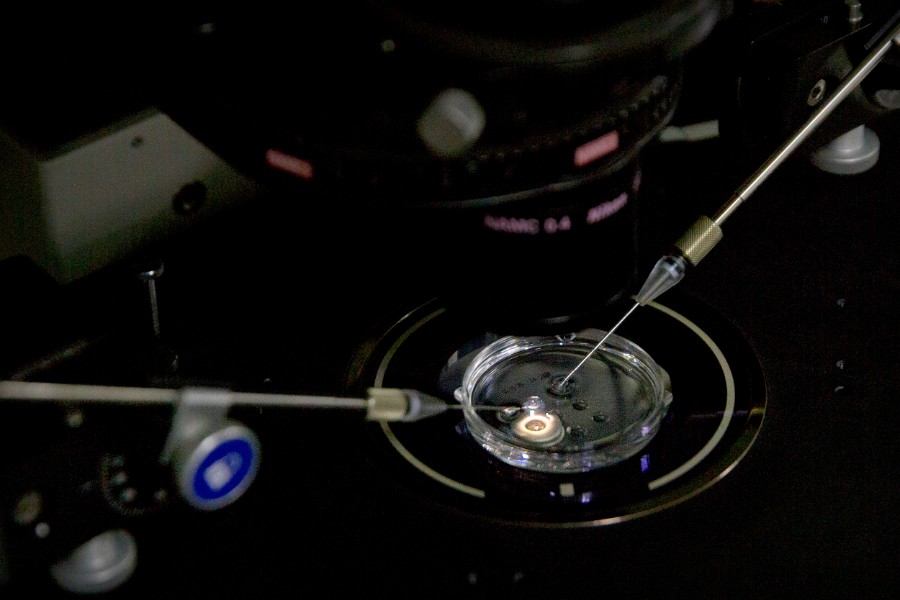
«Ножницы» для редактирования людей
CRISPR/Cas9 — это «молекулярные ножницы», противовирусный инструмент иммунитета одноклеточных, не имеющих клеточного ядра, — архей и бактерий. Существа с выраженным клеточным ядром — эукариоты, к которым относятся и люди, — такого инструмента не имеют. В 2013 году эти «ножницы» предложили использовать, чтобы сравнительно точно переносить нужные гены в нужные места ДНК эукариот, в том числе человека.
Методы редактирования генома были и раньше, но очень неточные и при этом дорогие. CRISPR/Cas9 оказался надежнее и эффективнее, чем его предшественники, однако в нескольких десятках процентов случаев при попытке отредактировать элемент ДНК система редактирует не только нужный участок, но и другие — ученые называют это «нецелевым редактированием». Другая проблема метода в том, что CRISPR/Cas9 не может отредактировать одинаковым образом все клетки того или иного организма или ткани: где-то редактирование получится, а где-то ДНК останется неизменной.
Осенью 2018 года биолог Цзянькуй Хэ заявил, что отредактировал этим методом геномы двух девочек под условными именами Нана и Лулу. В их ДНК внесли мутацию, повышающую устойчивость к ВИЧ, который был у одного из родителей девочек. Из-за несовершенства метода организмы обеих девочек, по словам самого Цзянькуй Хэ, получились «мозаичными»: в части их клеток есть ген, повышающий устойчивость к ВИЧ, а в части — нет. Эксперимент не получил планируемый результат, но поднял вопрос о генетическом редактировании эмбрионов.
Как избавиться от ошибок генетического редактирования?
По словам Дениса Ребрикова, его группа в ближайшие месяцы планирует провести редактирование гена в эмбрионе ребенка, полученного методом ЭКО от двух слабослышащих родителей. У каждого из них есть мутация в гене GJB2, которая приводит к глухоте. В обычной ситуации ребенок также бы имел нарушения слуха, но CRISPR/Cas9 позволит ввести пропущенный нуклеотид в ген GJB2, и младенец сможет слышать.
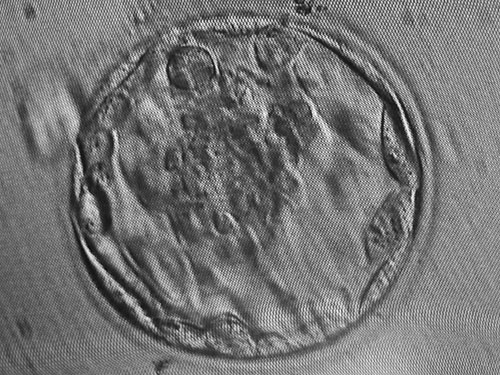
Чтобы убедиться, что редактирование будет успешным — без мозаицизма и нецелевых, случайных изменений в геноме будущего ребенка, группа Ребрикова сначала проведет проверочные эксперименты. Для супружеской пары это будет выглядеть как обычное экстракорпоральное оплодотворение (ЭКО): после гормональной терапии у женщины заберут яйцеклетки, затем в лаборатории их оплодотворят сперматозоидами ее мужа. Так будет получено десять зигот (одиночных клеток, из которых вырастают эмбрионы, — прим. ТД), каждая из которых потенциально может вырасти в эмбрион.
На стадии зиготы все десять клеток отредактируют с помощью CRISPR/Cas9, заполнив пропуск в их гене GJB2. Зиготам дадут расти пять суток до превращения в бластоцисту — шарик из 250 клеток. Именно такой путь в первые пять суток развития проходит и обычный эмбрион при естественном оплодотворении. На пятые сутки клетки всех десяти бластоцист подвергнут секвенированию, то есть «прочтению» последовательности ДНК. Процесс уничтожит клетки бластоцист, но даст в руки исследователей довольно точную последовательность отредактированной ДНК. Дальше ученые сравнят эту последовательность с неотредактированной ДНК обоих родителей и выяснят, насколько они отличаются и нет ли в геноме эмбрионов следов сбоев, типичных для метода CRISPR/Cas9.
Поскольку «прочитать» геном по одной клетке крайне сложно, куда эффективнее изучать множество клеток, чтобы снизить ошибки «прочтения». Группа Ребрикова планирует получить полный геном по 250 клеткам бластоцисты, то есть теоретически количество клеток с «прочитанной» ДНК будет достаточным, чтобы полноценно сравнить его с родителями.
ДНК ребенка в норме содержит примерно сотню мутаций, которых нет у его родителей, отмечает Денис Ребриков. Исследователи перейдут к следующему этапу эксперимента, если будут соблюдены все три условия: полный геном почти всех эмбрионов, например, девяти из десяти, содержит нормальное количество случайных мутаций; в нем нет следов ошибок «молекулярных ножниц» CRISPR/Cas9 и нет следов мозаицизма, все клетки почти всех бластоцист имеют «отремонтированную» ДНК.
Ученые используют другие яйцеклетки и сперматозоиды той же пары для получения новых зигот, где будет повторено то же редактирование «молекулярными ножницами», но уже для того, чтобы избавить потенциального ребенка от глухоты. На пятые сутки у каждой из таких бластоцист возьмут пять-семь клеток на биопсию, чтобы проверить, нет ли в них нецелевых изменений или мозаицизма. Эта биопсия не повредит бластоцистам: клетки забирают из ее отростка, некритичного для развития эмбриона в целом. Подобная биопсия проводится при ЭКО для большого количества родителей с опасными наследственными заболеваниями. На сегодня эта процедура давно отработана и считается безопасной.
«Большое “но”, — отмечает Денис Ребриков, — мы ориентируемся на то, что у нас весь эмбрион такой же, как эти пять клеток, лишь на основании первого эксперимента, где мы показали, что в целом весь эмбрион [генетически] одинаковый и мозаицизма нет, или он очень низкий… допуская, что анализа пяти клеток достаточно, чтобы судить о всем эмбрионе».
Если и на этих эмбрионах не будет следов нецелевого редактирования ДНК и мозаицизма, то лучший из таких эмбрионов будет пересажен в матку будущей матери. Эта схема выглядит более безопасной по сравнению с экспериментом китайского ученого — нет никаких данных о том, что Цзянькуй Хэ проводил полногеномное сравнение такого рода.
Корреспондент ТД спросил Дениса Ребрикова, не опасается ли он, что эксперимент на эмбрионе человека приведет к неожиданным последствиям в будущем, в том числе к проблемам со здоровьем у ребенка? Подобный печальный опыт генетического редактирования был: попытки клонировать обезьян 20 лет подряд приводили к их гибели сразу после рождения. Можно ли, не проведя опыты на животных, в том числе приматах, надеяться на отсутствие сходных проблем при использовании CRISPR/Cas9 на людях? Ученый отмечает: «На этот вопрос очень сложно ответить прямо». По его словам, если в эмбрионе чтение ДНК не покажет аномальных последствий редактирования, то с точки зрения научного метода нет никаких оснований ожидать каких-либо проблем. «Если мы с чем-то таким и столкнемся, то с чем-то совершенно неизвестным», — говорит исследователь.
«На другой чаше весов — тяжесть всех возможных ошибок метода»
«Такие дела» обратились к заведующему лабораторией геномной инженерии МФТИ Павлу Волчкову, чтобы узнать, как другие ученые оценивают инициативу группы Ребрикова. Волчков осторожно усомнился в своевременности такого эксперимента: «Методологически я не вижу здесь ничего сложного, вопрос в эффективности. Эффективность и безопасность метода CRISPR/Cas9 еще недостаточны, чтобы это можно было использовать на людях», — считает он.
Павел Волчков отмечает, что попытки геномного редактирования эмбриона пока даже не предпринимаются на Западе по довольно веским причинам. Права на CRISPR-методы проданы крупным биотехнологическим компаниям, и никто из них не пойдет на редактирование эмбриона человека. «Это коммерчески бессмысленно, — комментирует ученый и поясняет, что западные власти не дадут сертифицировать такой метод лечения на нынешнем этапе развития научных знаний. — Кроме того, это еще и огромные имиджевые риски, потому что корпорации считают, что это слишком рано делать. Если вы хотите поставить крест на своей компании, в которую вы вбухали пару миллиардов долларов, ну, тогда идите и редактируйте человеческий эмбрион. Вашу компанию просто закроют. FDA (правительственное Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США, — прим. ТД) придет, и вам такое устроят…»
Ученый отмечает, что сложно оценить, позволят ли российские власти группе Ребрикова редактировать гены эмбрионов. «На одной чаше весов — возможность стать если не первыми, то вторыми в мире, кто отредактировал геном человека, опередив в этом отношении все западные страны, — рассуждает он. — Более того, если бы все прошло хорошо, то группе Ребрикова удалось стать первой в мире, кто отредактировал геном “нормально”, не завалив все дело мозаицизмом, как в китайском эксперименте. Излечение от глухоты — вполне реальное достижение. На другой чаше весов — тяжесть всех возможных ошибок метода, если их вдруг не удастся отследить полностью».
Финальное решение о разрешении эксперимента Ребрикова будет принимать комитет по этике Научного центра гинекологии и акушерства имени Кулакова, считает Волчков. Однако он прогнозирует, что этический комитет захочет разделить ответственность с Минздравом, а последний не пожелает рисковать и «замылит всю эту активность».
По личной оценке Павла Волчкова, эксперимент преждевременный, потому что он «не видел убедительных результатов того же методах на мышах». Метод CRISPR/Cas9 для редактирования человеческого генома еще не готов, считает исследователь, но «с жаждой научной славы трудно что-то поделать», поэтому попытки такого редактирования будут предприниматься еще до созревания технологии.
Ученый добавляет, что на мышах ведутся схожие опыты, но технически проводить их в России не так просто, как на эмбрионах людей из-за нехватки вивариев. «Вот мы (группа лаборатории Волчкова, прим. ТД) лечим как раз мышей… но у нас вивариев в стране мало, а вот ЭКО-центров полным-полно, и ЭКО делают часто», — говорит он. На вопрос ТД: «Раз у нас в стране нет условий для экспериментов над мышами, то идут эксперименты на людях?», ученый ответил: «Вам смешно, но все звучит ровно так».
Каждый день мы пишем о самых важных проблемах в нашей стране. Мы уверены, что их можно преодолеть, только рассказывая о том, что происходит на самом деле. Поэтому мы посылаем корреспондентов в командировки, публикуем репортажи и интервью, фотоистории и экспертные мнения. Мы собираем деньги для множества фондов — и не берем из них никакого процента на свою работу.
Но сами «Такие дела» существуют благодаря пожертвованиям. И мы просим вас оформить ежемесячное пожертвование в поддержку проекта. Любая помощь, особенно если она регулярная, помогает нам работать. Пятьдесят, сто, пятьсот рублей — это наша возможность планировать работу.
Пожалуйста, подпишитесь на любое пожертвование в нашу пользу. Спасибо.
Помочь нам